广西普通高等教育专升本考试大纲与说明
(生物与化工大类)(2025 年版)
广西普通高等教育专升本考试(以下简称专升本考试)
贯彻党的教育方针,落实立德树人根本任务,是普通高校全
日制高职(专科)应届毕业生升入普通本科高校和本科层次
职业学校的选拔性考试,旨在促进高素质技术技能人才成
长,培养德智体美劳全面发展的社会主义建设者和接班人。
考试目的是科学、公平、有效地测试考生在高职(专科)阶
段相关专业知识、基本理论与方法的掌握程度和运用所学知
识分析问题、解决问题的能力,以利于各本科院校择优选拔,
确保招生质量。
生物与化工大类专业基础综合课考试包括无机化学、化
学分析和有机化学 3门课程,无机化学注重考查考生对无机
化学基础知识、基本理论的掌握程度和化学反应的相关计算
能力;化学分析注重考查考生对定量化学分析基础知识的掌
握程度和化学分析的实验技能;有机化学注重考查考生对有
机化合物基础知识、基础理论的掌握程度和相关应用能力、
实验能力。
一、考查内容
(一)无机化学
1.物质及其变化
(1)掌握理想气体状态方程,理想气体分压定律和分体
积定律;
(2)掌握稀溶液的依数性,掌握物质的量浓度、质量分
数、质量摩尔浓度、摩尔分数等概念及相互换算的方法;
(3)了解热力学的基本概念、热化学反应方程式;
(4)掌握化学反应的标准摩尔焓变、标准摩尔熵变和标
准摩尔吉布斯自由能变的计算方法。
2.化学反应速率和化学平衡
(1)了解化学反应速率,基元反应和非基元反应,质量
作用定律;
(2)了解温度对反应速率影响的阿伦尼乌斯经验式;
(3)了解化学平衡的特征;
(4)掌握标准平衡常数和标准吉布斯自由能变之间的
关系;
(5)能写出不同类型反应的标准平衡常数表达式,并能
应用标准平衡常数进行有关化学平衡的计算;能运用多重平
衡规则求标准平衡常数;
(6)了解温度对标准平衡常数的影响;
(7)掌握影响平衡移动的因素;
(8)掌握化学平衡移动的定性判据。
3.电解质溶液和离子平衡
(1)了解强电解质、弱电解质溶液;
(2)掌握水的解离和溶液 pH 的计算;
(3)掌握一元弱酸、弱碱的解离平衡的计算;
(4)了解缓冲溶液原理及缓冲溶液的组成和性质;
(5)掌握缓冲溶液 pH 的计算;
(6)了解同离子效应和盐效应对解离平衡的影响;
(7)理解难溶电解质沉淀溶解平衡的特点,会运用溶度
积规则判断沉淀溶解平衡的移动方向及进行有关计算。
4.氧化还原反应与电化学
(1)掌握氧化还原反应的基本概念及氧化还原反应方
程式的配平;
(2)掌握原电池的组成、电极反应、电池符号,了解电
极电势的概念及影响因素;
(3)掌握能斯特方程,能根据能斯特方程求非标准状态
下氧化还原反应的电池电动势;
(4)掌握原电池电动势与电池反应的关系,标准电动势
与氧化还原反应标准平衡常数的关系;
(5)能应用标准电极电势判断氧化剂和还原剂的强弱,
能用电极电势判断氧化还原反应的方向和完成程度;
(6)能运用元素电势图判断处于中间价态物质能否发
生歧化反应。
5.原子结构与元素周期律
(1)了解核外电子运动的特性——波粒二象性、不确定
原理、波函数与原子轨道,了解原子轨道和电子云角度分布
图和径向分布图;
(2)了解四个量子数的物理意义、相互关系及合理组
合;
(3)掌握核外电子排布的原则,能熟练写出前四周期原
子核外电子排布式;
(4)掌握元素的周期、元素的族及元素的分区;
(5)结合原子结构和周期表,了解电离能、电负性、原
子半径等概念及递变规律。
6.分子结构与固体结构
(1)了解价键(电子配对)理论,共价键的特性;
(2)理 解 σ 键和 π 键,杂化轨道理论的要点,杂化轨道
的类型和简单分子的空间构型关系;
(3)了解分子间作用力(如范德华力、氢键)及其对物
质物理性质(熔沸点、溶解度等)的影响;
(4)了解晶体的分类、不同类型晶体的结构特征和物理
性质。
7.配位化合物
(1)了解配合物、螯合物的概念以及配合物的组成;
(2)掌握配合物的命名;
(3)了解配合物价键理论的要点,了解配位键的形成条
件。
(二)化学分析
1.定量分析基础
(1)了解分析化学的分类方法,提高分析结果准确度的
方法;
(2)掌握定量分析的误差,定量分析结果的数据处理,
有效数字及其运算规则。
2.滴定分析基础
(1)了解滴定反应的条件与滴定方式,基准物质和标准
溶液,标准溶液浓度的表示方法;
(2)掌握滴定分析的基本计算,滴定分析实验的基本操
作规范。
3.酸碱滴定法
(1)了解酸碱平衡的理论基础,一元酸碱滴定的基本原
理及条件的选择,一元强酸强碱标准溶液的配制与标定;
(2)掌握一元酸碱溶液 pH 值的计算,常用酸碱指示剂
的变色原理及变色范围,酸碱滴定法的应用及计算。
4.配位滴定法
(1)了解金属 EDTA 螯合物的特点,配位滴定过程及
滴定条件选择,提高配位滴定选择性的方法,配合物的稳定
常数;
(2)掌握 EDTA 的性质,影响配位平衡的主要因素,常
用金属指示剂的原理、种类和使用常见问题,配位滴定突跃
的影响因素,配位滴定法常用标准溶液配制和标定,主要滴
定方式应用实例和计算。
5.氧化还原滴定法
(1)了解电极电势、标准电极电势和条件电极电势的概
念及相互关系,电极电势的应用,氧化还原滴定过程及滴定
突跃的影响因素;
(2)掌握影响氧化还原反应速率的因素,氧化还原滴定
指示剂的类型和氧化还原指示剂的选择,高锰酸钾法、重铬
酸钾法、碘量法的反应原理、常用的标准溶液配制与标定及
主要应用实例和计算。
6.沉淀滴定法
(1)了解沉淀滴定法对沉淀反应的要求,银量法的特
点、滴定方式和测定对象;
(2)掌握莫尔法、福尔哈德法、法扬司法确定终点的方
法原理、滴定条件、应用范围和应用实例计算。
7.重量分析法
(1)了解重量分析法的原理、过程及特点,重量分析法
对沉淀、沉淀剂的要求,沉淀形式和称量形式的不同,沉淀
溶解度的影响因素,影响沉淀纯度的因素,沉淀的条件和称
量形的获得;
(2)掌握重量分析法换算因数计算和应用实例结果计
算。
(三)有机化学
1.有机化合物及有机反应类型分类
(1)了解有机化合物的分类和定义、有机化合物的性质
特点、了解有机反应类型;
(2)掌握结构式、结构简式、键线式等有机物结构的书
写方法,掌握有机化学反应方程式的书写规则。
2.烷烃
(1)了解烷烃的同系物和同分异构概念;了解烷烃的物
理性质中熔沸点的变化规律,能够用分子间力进行解释;了
解有机物的同分异构体的分类;
(2)掌握烷烃的系统命名法,掌握烷烃的一溴代和一氯
代反应。
3.烯烃
(1)了解烯烃的结构,了解烯烃亲电加成的马氏规则;
(2)掌握烯烃的系统命名法、顺反异构体的命名和 Z-E
标记法;掌握烯烃的亲电加成、氧化、α-H 取代反应,烯烃
的制备,烯烃结构的推测与鉴别。
4.炔烃和二烯烃
(1)了解炔烃和二烯烃的结构,了解诱导效应、共轭效
应对化合物化学性质的影响;
(2)掌握炔烃和二烯炔的系统命名法,炔烃结构的推测
与鉴别;掌握炔烃的亲电加成,端炔氢对应的反应,共轭二
烯烃的 Diels-Alder 反应。
5.脂环烃
(1)了解脂环烃的分类,螺环、桥环烷烃的命名;了解
环烷烃由于角张力和扭转张力决定的稳定性差异;
(2)掌握单环烷烃和烯烃的系统命名法,掌握脂环烃的
加成反应、取代反应。
6.芳香烃
(1)了解苯的结构,了解定位规律的解释,了解不同定
位基对苯环亲电取代活性的影响;
(2)掌握单环芳香烃的结构和命名,掌握苯及其同系物
的亲电取代反应、氧化反应,掌握苯环亲电取代的定位规律
及应用。
7.卤代烃
(1)了解卤代烃的分类、同分异构现象、卤代烃的物理
性质,了解格氏试剂的制备和化学性质;
(2)掌握卤代烃的亲核取代反应,包括水解、醇解、氨
(胺)解、与硝酸银、氰化钾的反应,掌握卤代烃的消除反
应以及对应的查依采夫规则(Zaitsev Rule)。
8.醇、酚和醚
(1)了解醇、酚和醚的分类、结构;
(2)掌握醇、酚和醚的命名,掌握醇与活泼金属、卤化
氢的反应、酯化反应,醇的脱水、氧化和脱氢反应;
(3)掌握醇的鉴别,包括卢卡斯试剂法、与金属 Na 反
应等;掌握醚键断裂的反应规律;掌握酚的酸性、成醚、成
酯反应、酚芳环上的亲电取代;掌握酚的鉴别和分离。
9.醛和酮
(1)了解醛和酮的结构、分类;
(2)掌握醛和酮的系统命名法;掌握羰基亲核加成反
应,包括与格氏试剂的加成反应、羟醛缩合反应、还原反应、
歧化反应;掌握醛和酮 α-H 的反应,包括卤化、羟醛缩合反
应;掌握醛和酮的氧化和还原反应,包括氧化、催化加氢、
金属氢化物还原、Clemmensen 还原反应、Wolff-Kishner-黄鸣
龙反应、Cannizzaro 反应;掌握醛和酮的鉴别和分离方法,
包括银镜反应,与氨的衍生物反应等;掌握卤仿反应。
10.羧酸及其衍生物
(1)了解羧酸的结构、分类,了解羧酸衍生物的命名,
 了解羧酸衍生物的化学性质;
了解羧酸衍生物的化学性质;
(2)掌握羧酸的系统命名法;掌握羧酸的化学性质,包
括:酸性(羧酸、卤代酸)、羧酸衍生物的生成、羧基中羰基
还原为醇的反应、脱羧反应、α-H 的卤代反应;掌握羟基酸
的化学性质;掌握羧酸的鉴别和分离。
11.有机化学实验基础
(1)了解回流、蒸馏、分馏等有机实验的基本操作和基
本原理;
(2)能够搭建简单的有机化学反应装置并完成相关的
有机化学反应,能制备一些简单的有机化合物。
二、考试形式与试卷结构
(一)考试形式
闭卷(专业基础综合课合卷)、笔试。
(二)试卷分值及考试时间
满分 300 分,其中无机化学 100 分,化学分析 100 分,
有机化学 100 分。
考试时间 150 分钟。
(三)题型结构
课程 题型 题量、分值
单项选择题 12 题,每题 5 分,共 60 分。
无机化学 简答题 2 题,每题 10 分,共 20 分。
计算题 2 题,每题 10 分,共 20 分。
单项选择题 12 题,每题 5 分,共 60 分。
化学分析 计算题 2 题,每题 10 分,共 20 分。
综合题 1 题,20 分。

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 单项选择题 12 题,每题 5 分,共 60 分。
单项选择题 12 题,每题 5 分,共 60 分。
有机化学 简答题 2 题,每题 10 分,共 20 分。
综合题 1 题,20 分。
三、题型示例
(一)单项选择题
1.为了提高 CO 在反应 CO(g)+H2O(g)= CO2(g) + H2(g)
中的转化率,可采用的方法为
A.增加 CO 的浓度
B.增加水蒸气的浓度
C.按化学计量比增加水蒸气和 CO 的浓度
D.增大反应体系的总压
参考答案:B

参考答案:C
3.下列选项中,可用于制备格氏试剂的是
A.水 B.乙醚 C.氨水 D.甲醇
参考答案:B
(二)简答题
1.已 知 φӨ(Cl2/Cl-)=1.36 V,φӨ(Fe3+/Fe2+)=0.769 V。请判
断 Cl2、Cl-、Fe3+和 Fe2+四种物质中氧化性最强和还原性最强
的物质分别是什么。如将两电对组成原电池,请分别写出正
极和负极的电极反应式。
参考答案:
— 10 —
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 根据 φӨ(Cl2/Cl-)>φӨ(Fe3+/Fe2+)可知,
根据 φӨ(Cl2/Cl-)>φӨ(Fe3+/Fe2+)可知,
①氧化性最强的是 Cl2,还原性最强的是 Fe2+;
②正极:Cl2+2e- = 2Cl-
负极:2Fe2+-2e- = 2Fe3+
2.现有四个试剂瓶中分别装有无色的溴代正丁烷、丙烯
醇、乙醚和正丙醇,请通过化学方法(可选择不同的试剂),
根据实验现象,区分各个试剂瓶中的化合物。
参考答案:
从试剂瓶中取少量试剂,分别加入溴水,能观察到溴水
颜色褪去的是丙烯醇;再取少量未知试剂,分别加入 AgNO3
的醇溶液,能观察到有淡黄色沉淀产生的是溴代正丁烷;再
取少量未知试剂,分别加入金属 Na,能观察到有气泡产生的
是正丙醇,没有现象的是乙醚。
(三)计算题
1.计算 0.10 mol·L-1 NH4Cl 溶液的 pH 值和 NH4+的解离
度。(已知 Kbθ(NH3)= 1.8×10-5)
参考答案:
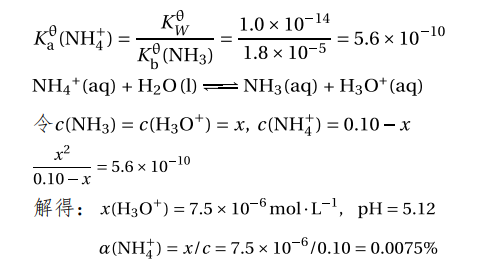
2.标定 NaOH 溶液实验中,称取邻苯二甲酸氢钾基准

![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]() 物 0.6156 g,加水溶解后以酚酞为指示剂,滴定至终点时消
物 0.6156 g,加水溶解后以酚酞为指示剂,滴定至终点时消
耗的 NaOH 溶液体积为 28.14 mL。计算 NaOH 溶液的浓度。
参考答案:
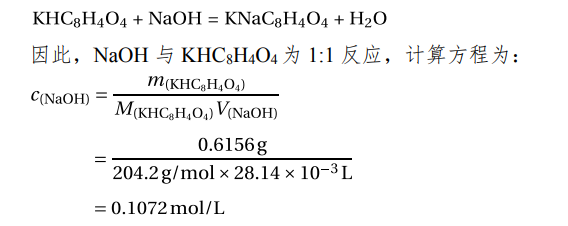
(四)综合题
1.请判断下列实验过程是否能达到实验目的,并说明原
因。
编号 实验目的 实验过程
A | 鉴别混合碱的 成分及各物质 的含量 | 先滴入 1~2 滴甲基橙指示剂,用 盐酸标准溶液滴定到终点;再滴 入 1~2 滴酚酞指示剂,继续用盐 酸标准溶液滴定到终点。 | |||||
B | 测定水的总硬 度 | 以钙试剂为指示剂,EDTA 为滴 定剂,滴定至终点,根据 EDTA 的用量计算水的总硬度。 | |||||
C | 证明 Fe2+具有 还原性 | 向较浓的 FeCl2 溶液中滴入少量 酸性 KMnO4 溶液,观察 KMnO4 溶液是否褪色。 | |||||
参考答案:
A:不能达到目的。应该先用酚酞指示剂,再用甲基橙指
示剂。如直接用甲基橙指示剂,则混合碱中所有的成分均已
跟盐酸反应完,再用酚酞不会有任何变化,且无法准确地表
达量的关系。
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
 B:不能达到目的。钙指示剂只能用于滴定水中的钙含
B:不能达到目的。钙指示剂只能用于滴定水中的钙含
量。而水的总硬度包括钙和镁的含量加和,应用铬黑 T 作为
指示剂。
C:不能达到目的。因为在酸性溶液中,FeCl2 中的 Cl-也
能使 KMnO4 溶液褪色,因此不能证明 Fe2+具有还原性。
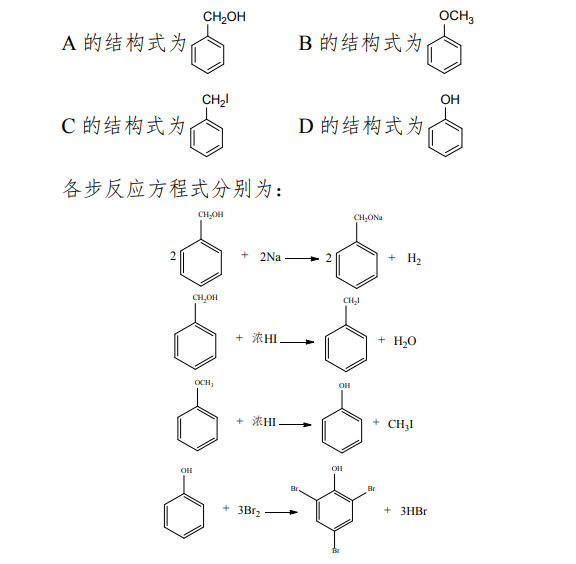
2.两个芳香族含氧化合物 A、B,化学式均为 C7H8O,
A 可与 Na 反应,而 B 不能。A 与浓 HI 反应生成 C(C7H7I),
B 用浓 HI 处理生成 D(C6H6O),D 遇溴水迅速产生白色沉
淀。写出 A、B、C、D 的结构式及各步反应方程式。
参考答案: